H ξηροφθαλμία αποτελεί μια πολυπαραγοντική ασθένεια της οφθαλμικής επιφάνειας που χαρακτηρίζεται κυρίως από απώλεια ομοιόστασης του δακρυϊκού φιλμ. Σήμερα, έχουμε περισσότερες θεραπευτικές επιλογές από ποτέ και υπάρχουν πολλές ακόμη σε εξέλιξη. Η επιτυχία οποιασδήποτε θεραπείας εξαρτάται από τη σωστή διάγνωση και εκτίμηση της υποκείμενης αιτιολογίας.
Η ξηροφθαλμία είναι μια διαταραχή της οφθαλμικής επιφάνειας που επηρεάζει εκατομμύρια ανθρώπους παγκοσμίως, με διαφορετική σοβαρότητα. Μπορεί να προκαλέσει ήπια συμπτώματα όπως μια απλή δυσφορία, μπορεί όμως να προκαλέσει και έντονες ενοχλήσεις έως πόνο, καθώς επίσης και διακύμανση της οπτικής οξύτητας. Με τον τρόπο αυτό επηρεάζει ουσιαστικά την ποιότητα ζωής που σχετίζεται με την όραση, περιορίζοντας έτσι δραστηριότητες όπως η οδήγηση, η ανάγνωση καθώς και η αναψυχή. Η ξηροφθαλμία επηρεάζει επίσης την παραγωγικότητα στο χώρο εργασίας καθιστώντας πιο δύσκολη τη χρήση ηλεκτρονικού υπολογιστή ή την ανάγνωση για παρατεταμένες περιόδους, τη μείωση στην ανοχή παραμονής σε ορισμένες περιβαλλοντικές συνθήκες καθώς επίσης και τη μείωση του χρόνου αποδοτικής εργασίας.
Τρέχουσες μελέτες εκτιμούν ότι περίπου 16,4 εκατομμύρια Αμερικανοί (6,8% του ενήλικου πληθυσμού των ΗΠΑ) έχουν διαγνωστεί με νόσο ξηρού οφθαλμού. Επιπλέον 6 εκατομμύρια (2,5% των ενηλίκων Αμερικανών) μπορεί να παρουσιάσουν συμπτώματα ξηροφθαλμίας αλλά δεν έχουν διαγνωστεί με νόσο του ξηρού οφθαλμού, τοποθετώντας το συνολικό εκτιμώμενο βάρος της νόσου στο 9,3% των ενηλίκων Αμερικανών. Επίσης, ο επιπολασμός του συνδρόμου είναι υψηλότερος στις γυναίκες σε σύγκριση με τους άνδρες και αυξάνεται με την ηλικία. Μια πρόσφατη πληθυσμιακή μελέτη διαπίστωσε επιπολασμό 11,3% σε όλους τους ενήλικες άνω των 50 ετών και έως 22,8% στις γυναίκες μεγαλύτερες από 75 ετών. Αξίζει σύντομα, επίσης, να αναφερθεί πως στις Ηνωμένες Πολιτείες, η ευρεία επικράτηση της ξηροφθαλμίας επιβάλλει σημαντική οικονομική επιβάρυνση, περίπου 3,8 δισεκατομμύρια δολάρια σε δαπάνες υγειονομικής περίθαλψης ετησίως. Κάθε χρόνο, το κοινωνικό κόστος που σχετίζεται με αυτή τη χρόνια πάθηση ανέρχεται σε περίπου 55 δισεκατομμύρια δολάρια στις Ηνωμένες Πολιτείες σύμφωνα με τελευταία στατιστικά.1 Επίσης, μεγάλες πολυκεντρικές μελέτες που έχουν διεξαχθεί στην Ευρώπη έχουν δείξει επιπολασμό 9,6% στο Ηνωμένο Βασίλειο (Twins UK Study) και 29,6% στη Γαλλία (Alienor Study).2,3
O πιο πρόσφατα ανανεωμένος όρος του συνδρόμου ξηρού οφθαλμού σύμφωνα με το Tear Film Ocular Surface (TFOS) Dry Eye Workshop (DEWS) II αναφέρει πως “Η ξηροφθαλμία είναι μια πολυπαραγοντική ασθένεια της οφθαλμικής επιφάνειας, που χαρακτηρίζεται από απώλεια ομοιόστασης του δακρυϊκού φίλμ και συνοδεύεται από οφθαλμικά συμπτώματα, στα οποία η αστάθεια του δακρυϊκού φίλμ, η υπερωσμοτικότητα, η φλεγμονή και η βλάβη της οφθαλμικής επιφάνειας καθώς επίσης και οι νευροαισθητήριες ανωμαλίες παίζουν αιτιολογικούς ρόλους”. Το σύνδρομο του ξηρού οφθαλμού είναι ένας όρος ομπρέλα που καλύπτει ένα πλήθος συμπτωμάτων και σημείων που σχετίζονται με μειωμένη οφθαλμική λίπανση, δηλαδή μειωμένη ποιότητα ή ποσότητα δακρύων στην οφθαλμική επιφάνεια. Ωστόσο, η απλή αυτή προσέγγιση του συνδρόμου δεν έχει καλύψει ούτε την επιστήμη αλλά ούτε και τους ασθενείς. Η ξηροφθαλμία έχει πολλές αιτίες, οι οποίες αλληλεπικαλύπτονται και αλληλοεπιδρούν. Σε άλλες περιπτώσεις είναι αποτέλεσμα άλλων παθολογικών καταστάσεων ή συνέπεια περιβαλλοντικών παραγόντων και φαρμάκων. Επίσης, σημαντικό είναι πως η ξηροφθαλμία είναι μια κατάσταση που μπορεί να προκληθεί ή να επιδεινωθεί από κάποιες οφθαλμικές χειρουργικές επεμβάσεις, χρήση υπολογιστή, χρήση φακών επαφής ή συνθήκες χαμηλής υγρασίας.
Η συστηματική διάγνωση και παρακολούθηση του συνδρόμου μπορεί να επιτευχθεί με τη χρήση διαφόρων επικυρωμένων μετρήσεων τόσο των σημείων όσο και των συμπτωμάτων της νόσου. Οι συνήθεις χρησιμοποιούμενες υποκειμενικές κλίμακες περιλαμβάνουν τον δείκτη οφθαλμικής επιφανείας (OSDI), το Ερωτηματολόγιο Ξηρών Οφθαλμών (DEQ) και την αξιολόγηση συμπτωμάτων iN Dry Eye (SANDE). Το OSDI είναι ένα ερωτηματολόγιο 12 ερωτήσεων που αξιολογεί τα συμπτώματα με βάση την τελευταία εβδομάδα προ εξέτασης. Οι βαθμολογίες κυμαίνονται από 0-100 με υψηλότερες βαθμολογίες που δείχνουν πιο σοβαρή ασθένεια. Το SANDE χρησιμοποιεί μια οπτική αναλογική κλίμακα και ζητά από τους ασθενείς να αξιολογήσουν τόσο τη σοβαρότητα όσο και τη συχνότητα των συμπτωμάτων ξηροφθαλμίας. Σημαντική αξιολόγηση των συμπτωμάτων γίνεται επίσης και με το ερωτηματολόγιο DEQ-5. Το ερωτηματολόγιο αυτό αναπτύχθηκε με τον εξορθολογισμό των συνηθισμένων συμπτωμάτων στο DEQ για τη διάκριση μεταξύ ομάδων με ποικίλη αυτοαξιολογημένη σοβαρότητα της ξηροφθαλμίας. Πιο συγκεκριμένα, το DEQ-5 αποτελείται από 5 χαρακτηριστικά: συχνότητα υδαρών οφθαλμών, δυσφορία και ξηρότητα (κλίμακα 0-4) και ένταση δυσφορίας και ξηρότητας αργά την ημέρα (κλίμακα 0-5). Αυτά μπορεί να χρησιμοποιηθούν σε συνδυασμό με ευρήματα κλινικών εξετάσεων, όπως χρώση κερατοειδούς και επιπεφυκότα με φλουορεσκεΐνη ή / και πράσινη λισαμίνη, χρόνο διάσπασης του δακρυϊκού φιλμ και δοκιμές Schirmer. Χρήσιμες είναι επίσης οι δοκιμές με μέτρηση της ωσμωτικότητας του δακρυϊκού φιλμ και η δοκιμή MMP-9. Η υπέρυθρη απεικόνιση των μεϊβομιανών αδένων, μπορεί να είναι χρήσιμη για την αξιολόγηση της σοβαρότητας της δυσλειτουργίας των μεϊβομιανών αδένων.
Στη διαγνωστική προσέγγιση που έχει υιοθετηθεί από το τελευταίο DEWS II έχουμε τις ερωτήσεις triage, στη συνέχεια την ανάλυση των παραγόντων κινδύνου και μετά περνάμε στα διαγνωστικά τεστ. Συγκεκριμένα, επί θετικής συμπτωματολογίας η οποία προκύπτει μέσα από ένα από τα στανταρισμένα κλινικά ερωτηματολόγια του TFOS και συγκεκριμένα το OSDI και το DEQ-5, απαιτείται σύμφωνα με τα DEWS, η ανεύρεση θετικότητας σε ένα από τα 3 προτεινόμενα τεστ που δείχνουν διαταραχή στην ομοιοστασία της δακρυϊκής στιβάδας. Τα τεστ αυτά είναι ο χρόνος διάσπασης της δακρυϊκής στιβάδας (TBUT), η Ωσμωτικότητα και η χρώση (staining) της οφθαλμικής επιφάνειας. Eφόσον μπει η διάγνωση ακολουθεί η ταξινόμηση, προκειμένου να επιλεγεί η βέλτιστη πρακτική αντιμετώπισης. Έχοντας λοιπόν τα συμπτώματα και έναν από τους 3 markers της διαταραχής της ομοιόστασης της δακρυϊκής στιβάδας προχωράμε για τη κατηγοριοποίηση της ξηροφθαλμίας. Έτσι, απαιτούνται τεστ που δείχνουν την παθολογία των μεϊβομιανών ή της λιπιδικής στιβάδας, προκειμένου να κατηγοριοποιηθεί η νόσος ως evaporative ή ένα μειωμένο ύψος δακρυϊκού μηνίσκου (TMH), προκειμένου να κατηγοριοποιηθεί ως aqueous deficiency, ή κάποιος συνδυασμός των ανωτέρω.
Οι παραδοσιακές θεραπείες του συνδρόμου περιλαμβάνουν τεχνητά δάκρυα χωρίς ιατρική συνταγή, ζεστές κομπρέσες και υγιεινή βλεφάρων. Ωστόσο, η παθολογία της νόσου της οφθαλμικής επιφάνειας διέπεται από έναν φαύλο κύκλο. Από τον ορισμό είναι ξεκάθαρη η ανάγκη ύπαρξης ομοιοστασίας στην οφθαλμική επιφάνεια και κατ’ επέκταση στη δακρυϊκή στιβάδα. Όταν λοιπόν κάτι λάθος συμβαίνει, το ερέθισμα σπάει την ομοιοστασία και η οφθαλμική επιφάνεια δεν μπορεί να προσαρμοστεί, μπαίνοντας σε έναν αυτοδιατηρούμενο θα έλεγε κανείς φαύλο κύκλο. Στη συνέχεια αυτό το ερέθισμα μπορεί να εξαφανιστεί αλλά ο φαύλος κύκλος παραμένει εκδηλώνοντας τελικά τη νόσο. Ακόμα και αν απομακρύνουμε το ερέθισμα ενδέχεται αυτός ο αυτοτροφοδοτούμενος κύκλος να συνεχίζει. Μια από τις πιο σημαντικές παραμέτρους αντιμετώπισης είναι η διαχείριση της φλεγμονής. Αν αυτή δεν σπάσει, είναι θέμα χρόνου να υποτροπιάσει η νόσος. Αυτό μπορεί να γίνει με στεροειδή, με κυκλοσπορίνη, και per os είτε με Ω-3 είτε με δοξυκικλίνη.
Η τοπική χρήση Κυκλοσπορίνης Α (CsA) αποτελεί μια θεραπευτική προσέγγιση σε περιπτώσεις που απαιτείται μακροχρόνια αντιφλεγμονώδη αγωγή ή που τα στεροειδή αντενδείκνυνται. Πρόκειται για έναν κυκλικό πολυπεπτιδικό ανοσορρυθμιστικό παράγοντα με ανοσοκατασταλτικές ιδιότητες, που έχει βρει χρήση ως αντιφλεγμονώδες φάρμακο λόγω της ικανότητάς του στη μείωση της ενεργοποίησης των Τ-κυττάρων με μεσολάβηση της IL-2. Έλαβε έγκριση από τον FDA για το σύνδρομο του ξηρού οφθαλμού το 2003. Η κυκλοσπορίνη δρα σε μοριακό επίπεδο δημιουργώντας σύμπλοκο με μια κυτταροπλασματική πρωτεΐνη, την κυκλοφιλίνη και το οποίο συνδέεται με μια συγκεκριμένη ενδοκυττάρια φωσφατάση, την καλσινευρίνη, την οποία και αναστέλλει εκλεκτικά. Η αναστολή της καλσινευρίνης και η επακόλουθη αναστολή του μεταγραφικού παράγοντα NFATc στα Τ-λεμφοκύτταρα, έχει ως αποτέλεσμα την περαιτέρω αναστολή της μεταγραφής και της μετάφρασης κυρίως του γονιδίου της IL-2, που οδηγεί σε αναστολή της διαφοροποίησης και του πολλαπλασιασμού των T-κυττάρων. Παράλληλα, αυξάνει την έκφραση του TGF-2, ενός παράγοντα που με τη σειρά του και αυτός αναστέλλει την IL-2. Επιπλέον, η κυκλοσπορίνη αναστέλλει την απελευθέρωση της ισταμίνης από τα μαστοκύτταρα και μειώνει την έκφραση διαφόρων κυτταρικών μορίων προσκόλλησης (ICAM), ενισχύοντας την αντιφλεγμονώδη δράση της. Η κυκλοσπορίνη ξεκίνησε εμπορικά να κυκλοφορεί με συγκέντρωση 0,05%, έχει ωστόσο εμφανιστεί στην αγορά και μια καινούρια γκάμα σκευασμάτων με διαφορετικές συγκεντρώσεις, καθώς επίσης και διαφορετικές τεχνικές προδιαγραφές παρασκευής και βιοδιαθεσιμότητας. Έχει εμφανιστεί στην αγορά τα τελευταία χρόνια η κυκλοσπορίνη με την τεχνολογία του νανογλακτώματος. Τα γαλακτώματα είναι μια μίξη 2 μη αναμίξιμων υγρών, ενός με βάση το νερό και ενός με βάση το λάδι. Με τη βοήθεια ενός γαλακτοματοποιητή που διαθέτει ένα υδρόφιλο και ένα λιπόφιλο άκρο, συνδέoνται αυτά τα δύο στοιχεία μεταξύ τους σε μια δομή λαδιού περιβαλλόμενο από νερό. Αυτή η τεχνολογία έχει εξελιχθεί σε νανογαλάκτωμα. Συγκεκριμένα, έχει κατασκευαστεί η τεχνολογία Novasorb με την οποία επιφανειοδραστικοί παράγοντες σταθεροποιούν μίγμα λιπαντικών και νερού μειώνοντας την επιφανειακή τάση στο σημείο επαφής. Πρόκειται για ένα κατιονικό γαλάκτωμα. Με το δεδομένο ότι η επιφάνεια του ματιού είναι φορτισμένη αρνητικά αντιλαμβάνεται κανείς ότι το κατιονικό διάλυμα έλκεται, με συνέπεια την αύξηση του χρόνου κατακράτησης, ενώ παράλληλα βελτιώνεται με τον τρόπο αυτό και η διασπορά του εναιωρήματος στην οφθαλμική επιφάνεια.
Δυστυχώς όμως, καμία θεραπεία δεν είναι βέλτιστη για όλους τους ασθενείς. Για τον λόγο ότι με τις τρέχουσες διαθέσιμες θεραπείες, τα σημεία και τα συμπτώματα του ασθενούς μπορούν να μειωθούν, αλλά ορισμένοι ασθενείς εξακολουθούν να αντιμετωπίζουν κάποια ενοχλητικά σημεία και συμπτώματα, η επιστήμη αναζητά όλο και περισσότερες νέες διαθέσιμες θεραπευτικές προσεγγίσεις. Οι νέες θεραπευτικές προσεγγίσεις περιλαμβάνουν αρχικά τα τοπικά φάρμακα και στοχεύουν στη μείωση των φλεγμονωδών διαμεσολαβητών και επομένως είναι πιθανότατα πιο αποτελεσματικά σε ασθενείς με ενδείξεις σημαντικής φλεγμονώδους αντίδρασης στα πλαίσια του συνδρόμου, όπως ασθενείς με μέτρια έως σοβαρή ανεπάρκεια δακρύων (με ή χωρίς σύνδρομο Sjogren) ή ασθένεια μοσχεύματος έναντι ξενιστή.
Lifitegrast
Τον Ιούλιο του 2016, το lifitegrast 5% πήρε έγκριση από τον FDA ως τοπικό αντιφλεγμονώδες φάρμακο για τη θεραπεία του συνδρόμου ξηρού οφθαλμού. Το φάρμακο μιμείται το μόριο διακυτταρικής προσκόλλησης-1 (ICAM-1), μπλοκάροντας τις αλληλεπιδράσεις μεταξύ του ICAM-1 και του λειτουργικά σχετιζόμενου με το λεμφοκύτταρο αντιγόνου-1 (LFA-1), τα οποία είναι καθοριστικά για την ενεργοποίηση και τη μετανάστευση των Τ-λεμφοκυττάρων. Κλινικές δοκιμές τριών φάσεων III (OPUS 1-3) έδειξαν βελτίωση τόσο στα σημεία όσο και στα συμπτώματα του συνδρόμου. Συγκεκριμένα, σε μια συγκεντρωτική ανάλυση των μελετών OPUS-2 και OPUS-3, το lifitegrast βελτίωσε σημαντικά το αποτέλεσμα του πρωταρχικού συμπτώματος ξηρότητας οφθαλμού εντός 14 ημερών και διατήρησε αυτό το αποτέλεσμα σε μια συγκεντρωτική ανάλυση στα τελικά σημεία της μελέτης των 84 ημερών. Η ασφάλεια του lifitegrast αποδείχθηκε καλή στη μελέτη SONATA, η οποία ακολούθησε 331 ασθενείς (220 lifitegrast έναντι 111 εικονικού φαρμάκου) για ένα έτος και δεν ανευρέθηκαν σημαντικές ανεπιθύμητες ενέργειες. Επιπλέον, οι συγκεντρώσεις του lifitegrast στο πλάσμα παρέμειναν χαμηλές και δεν εμφανίστηκε συστηματική ανοσοκαταστολή ή τοπικές ευκαιριακές λοιμώξεις. Τα πλεονεκτήματα του τοπικού lifitegrast που προτείνονται από τις παραπάνω μελέτες περιλαμβάνουν σχετικά γρήγορη επίδραση, μακροχρόνια ασφάλεια και βελτίωση τόσο στα σημεία όσο και στα συμπτώματα του συνδρόμου. Ωστόσο, υπάρχουν πιθανές παρενέργειες, όπως ερεθισμός, πόνος και αντίδραση στο σημείο ενστάλαξης, μειωμένη οπτική οξύτητα και δυσγευσία. Είναι επίσης άγνωστο εάν η ταυτόχρονη χρήση lifitegrast με τοπικά κορτικοστεροειδή μπορεί να οδηγήσει σε ταχύτερη ανακούφιση από τα συμπτώματα, όπως έχει βρεθεί σε προηγούμενη έρευνα σχετικά με τη χρήση CsA σε συνδυασμό με κορτικοστεροειδή. Μελλοντικές μελέτες σχετικά με την αποτελεσματικότητα της ταυτόχρονης χρήσης της lifitegrast και της κυκλοσπορίνης απαιτούνται επίσης.
Παράγωγα αίματος
Τα τελευταία χρόνια, προϊόντα που προέρχονται από αιμοπετάλια έχουν βρει ευρεία χρήση στην επούλωση τραυμάτων και στην αναγέννηση των ιστών. Η εφαρμογή αυτών των προϊόντων στο σύνδρομο ξηρού οφθαλμού εκμεταλλεύεται τις ομοιότητες μεταξύ φυσικών δακρύων και ορού, συμπεριλαμβανομένων λιπιδίων, πρωτεϊνών, αντιμικροβιακών στοιχείων και αυξητικών παραγόντων. Πολλαπλές μελέτες έδειξαν ότι αυτόλογες και / ή αλλογενείς σταγόνες ορού, βελτιώνουν τόσο τα συμπτώματα όσο και τα αντικειμενικά σημεία του συνδρόμου. Πιο πρόσφατα, αυξήθηκε το ενδιαφέρον για τη χρήση άλλων προϊόντων που προέρχονται από αίμα, ειδικά του πλάσματος πλούσιο σε αιμοπετάλια (E-PRP) και πλάσματος πλούσιο σε αυξητικούς παράγοντες (PGRF). Αυτά τα νεότερα προϊόντα περιέχουν τρεις έως πέντε φορές τη συγκέντρωση των αιμοπεταλίων σε σύγκριση με τον ορό. Τα E-PRP και PGRF επίσης δεν περιέχουν λευκοκύτταρα, τα οποία είναι παρόντα στον ορό και μπορούν να αυξήσουν τα επίπεδα των προφλεγμονωδών κυτοκινών που είναι επιζήμια για την οφθαλμική επιφάνεια. Αυτές οι υψηλότερες συγκεντρώσεις αυξητικών παραγόντων και άλλων ευεργετικών παραγόντων μπορεί να οδηγήσουν σε σημαντικά θεραπευτικά αποτελέσματα στην οφθαλμική επιφάνεια.
Intense Pulsed Light (IPL)
Το IPL περιλαμβάνει στόχευση χρωστικοφόρων ή αγγειακών βλαβών με ορατό και υπέρυθρο φως, το οποίο, κατά την απορρόφηση, μετατρέπεται σε καταστρεπτική θερμότητα. Αν και χρησιμοποιείται κυρίως στη δερματολογία με έγκριση από τον FDA για τη θεραπεία των τελαγγειεκτασιών, ο Toyos με τους συνεργάτες του περιέγραψαν για πρώτη φορά ένα πρωτόκολλο θεραπείας για τη χρήση IPL σε ασθένειες ξηροφθαλμίας το 2005.4 Πιο συγκεκριμένα το IPL χρησιμοποιήθηκε ως θεραπεία για την υποχώρηση της ξηροφθαλμίας που προκαλείται από τη δυσλειτουργεία των μεϊβομιανών αδένων, καθώς επίσης και συχνά σε ασθενείς που πάσχουν από ροδόχρου ακμή. Η θεραπεία IPL περιλαμβάνει άμεση εφαρμογή 590nm φωτός στο δέρμα με ρυθμίσεις που κυμαίνονται από 8 J/cm2 έως 20 J/cm2, ανάλογα με τη σοβαρότητα της νόσου. Αποτέλεσμα της θεραπείας είναι η πήξη των υποκείμενων αιμοφόρων αγγείων που οδηγεί σε μείωση των φλεγμονωδών μεσολαβητών και τήξη του ιξώδους εκκρίματος των Μεϊβομιανών αδένων, επιτρέποντας βελτιωμένη ροή. Πρόσφατες μελέτες, έχουν δείξει αξιόλογη βελτίωση τόσο στα σημεία όσο και στα συμπτώματα του συνδρόμου, ενώ το IPL διαθέτει πλέον έγκριση από το FDA για θεραπευτική χρήση σε ασθενείς με ξηροφθαλμία.
Ενώ αυτά τα αποτελέσματα είναι ενθαρρυντικά για το ρόλο του IPL στη θεραπεία του συνδρόμου, υπάρχουν περιορισμοί στη χρήση του. Για παράδειγμα, μόνο το ελαφρώς χρωματισμένο δέρμα (Fitzpatrick Skin Types 1–4) είναι επιλέξιμο για θεραπεία IPL, καθώς παρενέργειες όπως η υπομελάγχρωση είναι πιο συχνές σε πιο σκούρους τύπους δέρματος. Τα άνω βλέφαρα επίσης δεν θεωρούνται ασφαλής στόχος λόγω του κινδύνου απορρόφησης φωτός από χρωματισμένες ενδοφθάλμιες δομές, όπως η ίριδα.
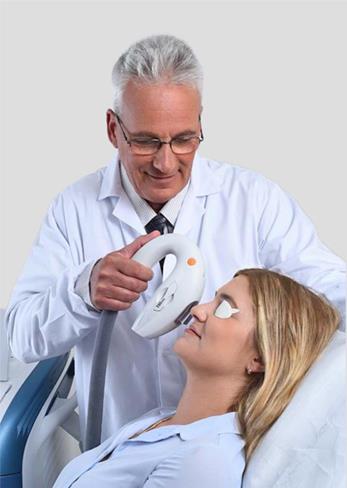
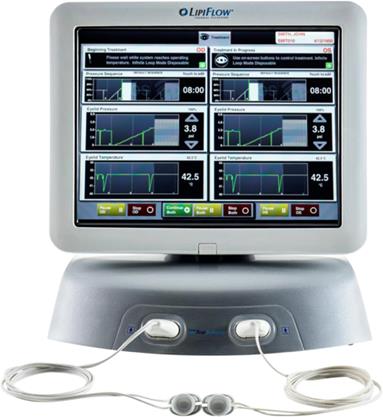
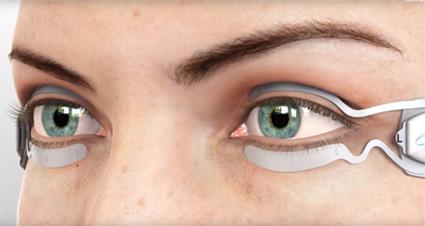
Vectored Thermal Pulsation (LipiFlow™)
Το LipiFlow ™ (TearScience, Morrisville, NC) είναι μια συσκευή που συνδυάζει την έκθλιψη των μεϊβομιανών αδένων με τη θερμότητα, σε μια τεχνική που αναφέρεται ως θεραπεία θερμικού παλμού φορέα, για την θεραπεία της δυσλειτουργίας των μεϊβομιανών αδένων. Κατά τη διάρκεια αυτής της διαδικασίας, η συσκευή εφαρμόζει θερμότητα πάνω από τον βολβικό επιπεφυκότα των άνω και κάτω βλεφάρων, παρέχοντας ταυτόχρονα παλμική εξωτερική πίεση. Οι Hagen et al. δημοσίευσαν μια προοπτική, τυχαιοποιημένη, παράλληλη ομάδα μελέτης που συγκρίνει την θεραπεία με LipiFlow™ και με μια 3μηνη πορεία δοξυκυκλίνης για τη θεραπεία της δυσλειτουργίας των μεϊβομιανών αδένων σε 28 ασθενείς.5 Μετά τη θεραπεία, οι βαθμολογίες SPEED βελτιώθηκαν και στις δύο ομάδες αλλά ήταν σημαντικά καλύτερες στη ομάδα LipiFlow ™ σε σύγκριση με την ομάδα δοξυκυκλίνης. Οι δύο ομάδες ήταν συγκρίσιμες στη βαθμολογία της λειτουργίας των μεϊβομιανών αδένων μετά τη θεραπεία, στο TBUT και στη χρώση του κερατοειδούς και του επιπεφυκότα με φλουρεσκεΐνη. Αυτά τα αποτελέσματα υποδηλώνουν ότι το Lipiflow ™ μπορεί να είναι μια θεραπεία εκλογής για ασθενείς με δυσλειτουργία μεϊβομιανών αδένων. Οι ανεπιθύμητες ενέργειες για το Lipiflow ™ είναι ελάχιστες και περιλαμβάνουν δυσφορία στα μάτια και τα βλέφαρα που επιλύονται αμέσως μετά τη θεραπεία.
Rexon® (Resono Ophthalmic, Sandrigo, Italy)
Ηλεκτρικό ρεύμα χαμηλής ισχύος και υψηλής συχνότητας χορηγείται από το Rexon-Eye®. Το Quantum Molecular Resonance (QMR) παράγει κύματα με συγκεκριμένη μορφή σε υψηλές συχνότητες (4–64 MHz) και χαμηλή ένταση μέσω ηλεκτρικών πεδίων.6 Υπάρχουν ενδείξεις ότι ο χειρισμός του ηλεκτρομαγνητικού περιβάλλοντος σε βιολογικά συστήματα ευνοεί τη διαδικασία επούλωσης τραυμάτων, τη μείωση της φλεγμονώδους αντίδρασης και την αγγειογένεση.7 Δεν έχει θερμικά αρνητικά αποτελέσματα και βελτιώσεις εμφανίζονται μετά από επαναλαμβανόμενες εφαρμογές σε συγκεκριμένα διαστήματα. Στην περίπτωση της ξηροφθαλμία, η υπόθεση είναι ότι το QMR είναι ικανό να διεγείρει το μεταβολισμό και τη φυσική αναγέννηση των κυττάρων εφαρμόζοντας ηλεκτρικά πεδία υψηλής συχνότητας χαμηλής ισχύος. Το τελικό αποτέλεσμα είναι η διέγερση του δακρυϊκού συστήματος και η «επανενεργοποίηση» των μεϊβομιανών αδένων.8,9 Δεδομένα δείχνουν ότι αυτή η συγκεκριμένη τεχνολογία μπορεί να αντιμετωπίσει αποτελεσματικά και με ασφάλεια τα συμπτώματα και τα σημεία του DED.8,9
Το πρωτόκολλο Rexon® προβλέπει τέσσερις συνεδρίες 20 λεπτών θεραπείας QMR, μία φορά την εβδομάδα. Η θεραπεία επιτυγχάνεται τοποθετώντας την ειδικά σχεδιασμένη ομοιόμορφη μάσκα επαφής πάνω στα κλειστά βλέφαρα μαζί με ειδικές, μιας χρήσης, αδιάβροχες λωρίδες που φοριούνται μεταξύ του ηλεκτροδίου της μάσκας και της επιφάνειας του βλεφάρου. Οι λωρίδες συμβάλλουν στην ομοιόμορφη εξάπλωση του ηλεκτρικού ρεύματος σε ολόκληρη την επιφάνεια των οφθαλμών, αυξάνοντας την ικανότητά του να φτάνει στους μεϊβομιανούς και δακρυϊκούς αδένες. Επιπλέον, οι ηλεκτρικές ιδιότητες του υλικού τους επιτρέπουν την ελαχιστοποίηση της έντασης ρεύματος ικανή να προκαλέσει το θεραπευτικό αποτέλεσμα QMR®. Μια προσαρμοσμένη κλίμακα μονάδας χρησιμοποιείται για την εμφάνιση της εφαρμοζόμενης ισχύος. Το Rexon® έχει κλίμακα μονάδας από 0 έως 10, με το 0 να αντιστοιχεί σε μηδενική ισχύ και 10 να αντιστοιχεί στη μέγιστη ισχύ.
MiBoThermoflo
Το Mibo Thermoflo (MiBo Medical Group, Dallas, TX) είναι μια θεραπευτική συσκευή για τη θεραπεία του συνδρόμου ξηρού οφθαλμού που σχετίζεται με τη δυσλειτουργία μεϊβομιανών αδένων, το οποίο στοχεύει στη μεγιστοποίηση της ρευστοποίησης και της έκκρισης του meibum, βελτιώνοντας έτσι την ποιότητα του δακρυϊκού φιλμ. Ο κατασκευαστής συνιστά τρεις θεραπείες, κάθε δύο εβδομάδες, και την αξιολόγηση των ασθενών μετά για να προσδιοριστεί εάν απαιτούνται μελλοντικές θεραπείες. Παρόλο που δεν έχουν δημοσιευτεί ακόμη μελέτες για την αποτελεσματικότητά του, τα προκαταρκτικά δεδομένα από μια δοκιμή που χρηματοδοτήθηκε από τον κατασκευαστή έδειξαν σημαντική βελτίωση στο TBUT, την ωσμωτικότητα, το SPEED και το OSDI τέσσερις μήνες μετά τη θεραπεία σε 51 ασθενείς. Ωστόσο, οι Kendrick & Alloo ανέφεραν σε μια μελέτη τους, ότι η θεραπεία ήταν αναποτελεσματική στην αύξηση της μέσης θερμοκρασίας του πάνω από τους 40 ° C, της θερμοκρασίας δηλαδή που απαιτείται για την αποτελεσματική ρευστοποίηση του εκκρίματος των μεϊβομιανών αδένων.10 Πρέπει να διεξαχθεί μια τυχαιοποιημένη, στοχευμένη κλινική δοκιμή ελέγχου της συγκεκριμένης θεραπείας για περαιτέρω διερεύνηση των αποτελεσματικότητα και ασφάλεια.
Το BlephEx™
Το BlephEx ™ (Scope Ophthalmics, London, UK) είναι μια θεραπεία για τη βλεφαρίτιδα συμπληρωματικά της υγιεινής βλεφάρων. Αυτή η φορητή συσκευή περιλαμβάνει έναν περιστρεφόμενο μικρο-σφουγγάρι μίας χρήσης για την απομάκρυνση των υπολειμμάτων από βλεφαρίδες και βλέφαρα. Οι Connor et al. κατέδειξαν τα θετικά αποτελέσματα του BlephEx ™ στη θεραπεία συμπτωμάτων ξηροφθαλμίας. Σε μια μικρή μελέτη 20 ασθενών, οι συγγραφείς διαπίστωσαν ότι η βαθμολόγηση της δυσλειτουργίας μεϊβομιανών αδένων και της βλεφαρίτιδας (χρησιμοποιώντας κλίμακα Efron Grading), TBUT και OSDI βελτιώθηκαν σημαντικά τέσσερις εβδομάδες μετά τη θεραπεία με BlephEx™.11
TearCare®
Το σύστημα TearCare® (Sight Sciences, Menlo Park, CA) είναι μια θεραπεία που είναι διαθέσιμη από το 2019 και η οποία στοχεύει στο συνδυασμό του θεραπευτικού αποτελέσματος της θεραπείας με θερμή έκθλιψη και της χειροκίνητης εκκένωση του αδένα για τη θεραπεία της δυσλειτουργίας των μεϊβομιανών αδένων. Η διαδικασία περιλαμβάνει τοποθέτηση, μιας χρήσης, iLid™ σε κάθε ταρσική πλάκα παρέχοντας σταθερή, ρυθμιζόμενη θερμότητα στους 41°C – 45°C σε διάστημα 12 λεπτών, κατά τη διάρκεια του οποίου ο ασθενής ενθαρρύνεται να ανοιγοκλείνει κανονικά τα βλέφαρα για να επιτρέπεται η φυσική έκφραση του meibum. Στη συνέχεια ακολουθείται χειροκίνητη έκθλιψη του meibum από τον ιατρό αμέσως μετά την αφαίρεση των iLid. Για τον λόγο ότι πρόκειται για μια πρόσφατη θεραπεία, πρέπει να διεξαχθούν στο μέλλον τυχαιοποιημένες και ελεγχόμενες με εικονικό φάρμακο κλινικές δοκιμές για περαιτέρω αξιολόγηση της αποτελεσματικότητας και της ασφάλειας του συστήματος TearCare®.
TrueTear®
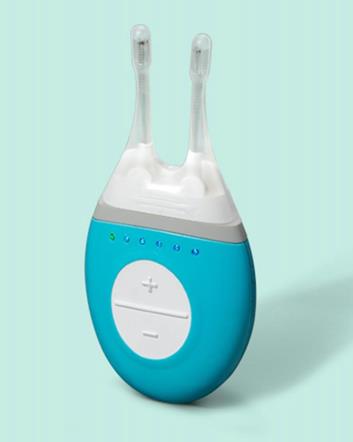
Μια σχετικά νέα συσκευή που έχει εγκριθεί από το FDA για τη θεραπεία του συνδρόμου ξηρού οφθαλμού είναι το Intranasal Tear Neurostimulator (ITN, TrueTear®, Allergan, plc). Το ITN σχεδιάστηκε για να διεγείρει τα βλεννογονικά νεύρα μέσω μικρών ηλεκτρικών ρευμάτων για να αυξήσει την παραγωγή φυσικών δακρύων μέσω της οδού αντανακλαστικής δακρυϊκής λειτουργίας. Η διέγερση των νευρικών ινών στο ρινικό βλεννογόνο έχει αποδειχθεί ότι αυξάνει την παραγωγή δακρύων. Αντίθετα, η έλλειψη διέγερσης αυτών των ρινικών βλεννογόνων ινών του τριδύμου νεύρου, όπως γίνεται χαρακτηριστικά σε ασθενείς με αφαίρεση του τριδύμου νεύρου, με μειωμένη ροή αέρα λόγω αλλεργίας ή με τραχειοστομία, έχει αποδειχθεί ότι οδηγεί σε μειωμένη παραγωγή δακρύων. Η συσκευή αποτελείται από δύο μικρούς ανιχνευτές, σχεδιασμένοι για να τοποθετείται ένας σε κάθε ρουθούνι, με πέντε επίπεδα έντασης διέγερσης να επιλέγονται από τον χρήστη.
Το 2016, οι Friedman et al. δημοσίευσαν τα αποτελέσματα μιας πιλοτικής μελέτης 40 ατόμων που χρηματοδοτήθηκε από την Allergan, στους οποίους δόθηκε εντολή να χρησιμοποιούν τη συσκευή ITN τέσσερις φορές την ημέρα για 180 ημέρες.12 Διαπιστώθηκε από τα αποτελέσματα ότι οι μέσες βαθμολογίες Schirmer ήταν σημαντικά υψηλότερες μετά τη ρινική διέγερση με τη συσκευή από ό, τι πριν από τη διέγερση και ότι οι βαθμολογίες του κερατοειδούς, του επιπεφυκότος και των οφθαλμικών συμπτωμάτων (όπως μετρήθηκε με το OSDI) μειώθηκαν σημαντικά από την έναρξη έως την ημέρα 180. Οι πιο συχνές ανεπιθύμητες ενέργειες της συσκευής ITN περιλαμβάνουν ρινική δυσφορία, καύση και πόνο, ρινορραγίες, παροδική ηλεκτρική δυσφορία, ρινική συμφόρηση, πόνος στο πρόσωπο και πονοκεφάλους. Επίσης, η συσκευή έχει αντένδειξη σε ασθενείς με καρδιακούς βηματοδότες ή άλλα εμφυτευμένα μεταλλικά ή ηλεκτρονικά είδη στην κεφαλή ή το λαιμό, χρόνιες ρινορραγίες ή άλλες καταστάσεις που μπορούν να προκαλέσουν αυξημένη αιμορραγία. Το κόστος της συσκευής μπορεί επίσης να είναι περιοριστικό, καθώς η συσκευή είναι περίπου 1000$ και η παροχή ανταλλακτικών μιας χρήσης είναι περίπου 50$, κανένα από τα οποία δεν καλύπτεται από τα περισσότερα ασφαλιστικά προγράμματα.
Αμνιακή μεμβράνη
Υπάρχουν επί του παρόντος δύο διαθέσιμες στο εμπόριο ποικιλίες, είτε κρυοσυντηρημένες στους −80 ° C, όπως το ProKera ™ (Bio-Tissue, Inc, Miami, FL) ή αποστειρωμένες αφυδατωμένες και αποθηκευμένες σε θερμοκρασία δωματίου, όπως το AmbioDisk ™ (Katena Products , Inc, Denville, NJ). Το ProKera ™ διατίθεται ως συσκευή που μπορεί να τοποθετηθεί στον οφθαλμό του ασθενούς και διαθέτει δακτύλιο που συγκρατεί τη μεταμόσχευση αμνιακής μεμβράνης (AMT) στη θέση της. Το πρωτότυπο ProKera ™ ενδείκνυται για μέτριες έως σοβαρές ενδείξεις, συμπεριλαμβανομένων των νευροτροφικών ελκών, της σοβαρής μολυσματικής κερατίτιδας, της θολερότητας μετά το PRK και της οζώδους εκφύλισης του Salzmann. Πρόσφατα, οι McDonald et al. δημοσίευσαν αποτελέσματα από 97 μάτια 84 ασθενών με σοβαρή ξηροφθαλμία, παρά τις μέγιστες συμβατικές θεραπείες, που υποβλήθηκαν σε θεραπεία με το ProKera ™ Slim. Μετά από διάρκεια θεραπείας 5,4 ημερών, το 88% είχε βελτιωμένη οφθαλμική επιφάνεια, χωρίς σοβαρές ανεπιθύμητες ενέργειες. Βέβαια, απαιτείται, περαιτέρω μελέτη για τον προσδιορισμό της διάρκειας της επίδρασης από την τοποθέτηση μεμβράνης, καθώς και σύγκριση των δύο διαθέσιμων προϊόντων.
Η όλο και μεγαλύτερη έκταση του προβλήματος της ξηροφθαλμίας την έχει αναδείξει ως μια από τις πλέον συχνές οφθαλμικές παθήσεις. Φαίνεται ότι η αγορά καθώς και η ευρύτερη διάσταση του προβλήματος της ξηροφθαλμίας ευνοούν και επιζητούν την ανάπτυξη θεραπευτικών επιλογών για την ξηροφθαλμία. Αναμένεται στο μέλλον να δούμε περισσότερες θεραπευτικές προσεγγίσεις στο πρόβλημα αυτό, τόσο σε επίπεδο φαρμακευτικών επιλογών, όσο και σε θεραπευτικές συσκευές.
Βιβλιογραφία
- Farrand KF, Fridman M, Stillman IO, Schaumberg DA. Prevalence of Diagnosed Dry Eye Disease in the United States Among Adults Aged 18 Years and Older. Am J Ophthalmol 2017; 182:90–98.
- Vehof, D. Kozareva, P.G. Hysi, C.J.Hammond Prevalence and risk factors of dry eye disease in a British female cohort Br J Ophthalmol, 98 (12) (2014), pp. 1712-1717
- Malet, M. Le Goff, J. Colin, C.Schweitzer, M.N. Delyfer, J.F. Korobelnik, et al. Dry eye disease in French elderly subjects: the Alienor Study Acta Ophthalmol, 92 (6) (2014), pp. e429-e436
- Toyos R, McGill W, Briscoe D. Intense pulsed light treatment for dry eye disease due to meibomian gland dysfunction; a 3-year retrospective study. Photomed Laser Surg 2015;33(1):41–46.
- Hagen KB, Bedi R, Blackie CA, Christenson-Akagi KJ. Comparison of a single-dose vectored thermal pulsation procedure with a 3-month course of daily oral doxycycline for moderate-to-severe meibomian gland dysfunction. Clin Ophthalmol 2018; 12:161–168.
- Liu Q, Song B. Electric field regulated signaling pathways Int J Biochem Cell Biol. 2014;55:264-8.
- Costin GE, Birlea SA, Norris DA. Trends in wound repair: cellular and molecular basis of regenerative therapy using electromagnetic fields. Curr Mol Med. 2012 Jan; 12(1):14-26.
- Ferrari G, Colucci A, Barbariga M, Ruggeri A, Rama P. High Frequency Electrotherapy for the Treatment of Meibomian Gland Dysfunction. Cornea. 2019 Nov;38(11):1424-1429
- Pedrotti E, Bosello F, Fasolo A, Frigo AC, Marchesoni I, Ruggeri A, Marchini G. Transcutaneous periorbital electrical stimulation in the treatment of dry eye. Br J Ophthalmol. 2017Jun;101(6):814-819
- Connor CG, Choat C, Narayanan S, Kyser K, Rosenberg B, Mulder D. Clinical Effectiveness of Lid Debridement with BlephEx Treatment. Investigative Ophthalmology & Visual Science. 2015;56(7):4440–4440
- Connor CG, Choat C, Narayanan S, Kyser K, Rosenberg B, Mulder D. Clinical Effectiveness of Lid Debridement with BlephEx Treatment. Investigative Ophthalmology & Visual Science. 2015;56(7):4440–4440
- McDonald MB, Sheha H, Tighe S, et al. Treatment outcomes in the DRy Eye Amniotic Membrane (DREAM) study. Clin Ophthalmol 2018; 12:677–681.
- O’Neil EC, Henderson M, Massaro-Giordano M, Bunya VY. Advances in dry eye disease treatment Curr Opin Ophthalmol. 2019 May;30(3):166-178.
- Buckley RJ.Eye Assessment and management of dry eye disease. (Lond). 2018 Feb;32(2):200-203.
- Marshall LL, Roach JM. Treatment of Dry Eye Disease Consult Pharm. 2016 Feb;31(2):96-106.
- Clayton JA. Dry Eye N Engl J Med. 2018 Jun 7;378(23):2212-2223.