Εισαγωγή
Η νόσος του Πάρκινσον (Parkinson’s Disease) αποτελεί μια προοδευτική νευροεκφυλιστική διαταραχή, με συνεχώς αυξανόμενη επίπτωση στον γηράσκοντα πληθυσμό. Κεντρικός παθοφυσιολογικός μηχανισμός της νόσου θεωρείται η ανώμαλη συσσώρευση α-συνουκλεΐνης στο κεντρικό νευρικό σύστημα, η οποία οδηγεί σε εκφύλιση των ντοπαμινεργικών νευρώνων, κυρίως στη μέλαινα ουσία.
Πέρα από τις κινητικές διαταραχές, η νόσος του Πάρκινσον σχετίζεται και με πρώιμα οπτικά συμπτώματα, όπως μείωση της οπτικής οξύτητας, εξασθένηση της ευαισθησίας στην αντίθεση (contrast sensitivity) και εμφάνιση οπτικών ψευδαισθήσεων. Τα συμπτώματα αυτά συχνά προηγούνται των κινητικών ή γνωσιακών διαταραχών και σχετίζονται με δυσλειτουργία τόσο του οπτικού φλοιού όσο και του αμφιβληστροειδούς, όπου η ντοπαμίνη, που λειτουργεί ως νευροδιαβιβαστής στην οπτική επεξεργασία, εμφανίζεται μειωμένη σε αυτούς τους ασθενείς.
Πρόσφατα, μελέτες έχουν αναδείξει ότι η νευροεκφύλιση συνοδεύεται και από μικροαγγειακές μεταβολές, οι οποίες φαίνεται να συμβάλλουν στην παθογένεια και εξέλιξη της νόσου. Λόγω της ανατομικής και εμβρυολογικής ομοιότητας του αμφιβληστροειδικού και του εγκεφαλικού μικροαγγειακού δικτύου, η μελέτη του αμφιβληστροειδούς παρέχει μια έμμεση μέθοδο εκτίμησης της μικροκυκλοφορίας του εγκεφάλου και κεντρικού νευρικού συστήματος.
Η Οπτική Τομογραφία Συνοχής με Αγγειογραφία (OCT-Aγγειογραφία) επιτρέπει την ποσοτικοποίηση της μικροκυκλοφορίας του αμφιβληστροειδούς και του χοριοειδούς, προσφέροντας νέα δεδομένα για την κατανόηση των νευροεκφυλιστικών νοσημάτων. Παράμετροι όπως η πυκνότητα αγγείων (Vessel Density / VD), η αιματική ροή (Flow Density / FD) και τα χαρακτηριστικά της αναγγείου ζώνης στην ωχρά (Foveal Avascular Zone / FAZ) φαίνεται να σχετίζονται με δομικές και λειτουργικές αλλοιώσεις στη νόσο του Πάρκινσον.
Σκοπός της παρούσας μελέτης ήταν η χαρτογράφηση των μικροαγγειακών αλλοιώσεων των έσω στιβάδων του αμφιβληστροειδούς στην περιοχή της ωχράς και του οπτικού νεύρου, σε ασθενείς με πρώιμο στάδιο νόσου του Πάρκινσον, με στόχο την ανάδειξη πιθανών βιοδεικτών για την πρώιμη διάγνωση και παρακολούθηση της νόσου.
Υλικό και Μέθοδοι
Η παρούσα μελέτη διεξήχθηκε στην Οφθαλμολογική Κλινική σε συνεργασία με τη Νευρολογική Κλινική του Πανεπιστημιακού Νοσοκομείου Ιωαννίνων, έπειτα από έγκριση της αρμόδιας επιτροπής δεοντολογίας.
Συμπεριλήφθηκαν ασθενείς με πρόσφατη διάγνωση νόσου του Πάρκινσον, η οποία επιβεβαιώθηκε από εξειδικευμένο νευρολόγο. Απαραίτητη προϋπόθεση για τη συμμετοχή ήταν το πρώιμο στάδιο της νόσου. Όλοι οι συμμετέχοντες υποβλήθηκαν σε γνωστική εκτίμηση με το τεστ MoCA. Εξαιρέθηκαν άτομα με ωχρική ή άλλη οφθαλμική/συστηματική πάθηση που θα μπορούσε να επηρεάσει την αμφιβληστροειδική κυκλοφορία. Ως ομάδα ελέγχου χρησιμοποιήθηκαν υγιή άτομα αντιστοιχισμένα ως προς την ηλικία και το φύλο.
Η απεικόνιση πραγματοποιήθηκε με τη χρήση του Zeiss Cirrus HD-5000 OCT με AngioPlex®. Για την περιοχή της ωχράς, χρησιμοποιήθηκε πρότυπο σάρωσης 6χ6 mm2 και αναλύθηκαν οι εξής παράμετροι στο επιπολής τριχοειδικό αγγειακό δίκτυο: αγγειακή πυκνότητα (vessel density), αιματική ροή (perfusion) και χαρακτηριστικά της ωχρικής αναγγείου ζώνης (επιφάνεια, περίμετρος, κυκλικότητα). Η περιοχή σάρωσης διαιρέθηκε αυτόματα σε τρεις υποπεριοχές: ωχρά (1 mm), παραωχρική (1–3 mm) και περιωχρική περιοχή (3–6 mm).
Για την κεφαλή του οπτικού νεύρου, χρησιμοποιήθηκε μοτίβο σάρωσης 4.5χ4.5 mm2 και αναλύθηκε η αιματική ροή στο περιθηλαίο τριχοειδικό αγγειακό δίκτυο μέσω ειδικών δεικτών πυκνότητας αιμάτωσης (perfusion density) και δείκτη ροής (flux index), όπως αναλύθηκαν με κατάλληλες μεθόδους.
Αποτελέσματα
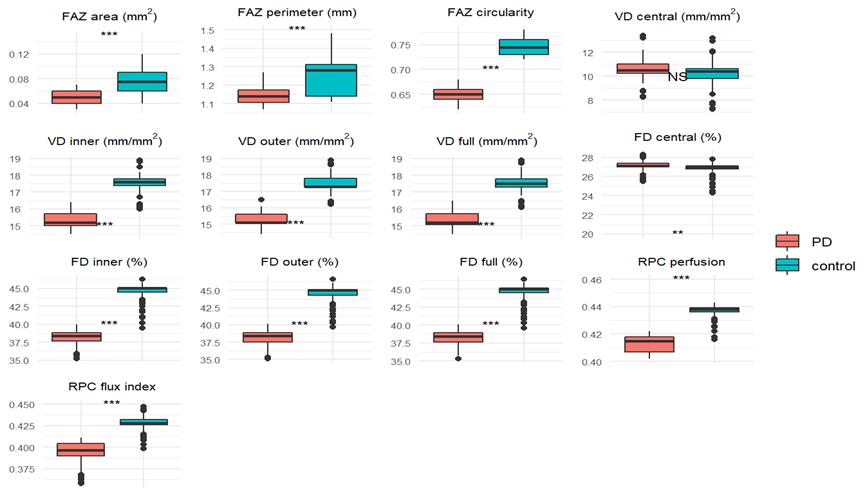
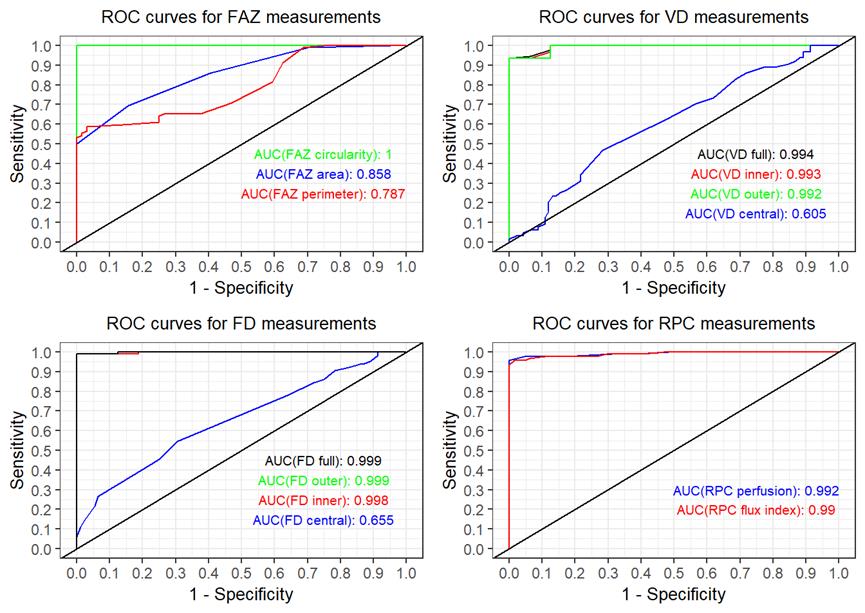
Οι ασθενείς με νόσο του Πάρκινσον εμφάνισαν σημαντικά μειωμένη αγγειακή πυκνότητα και αιματική ροή στο αγγειακό δίκτυο του επιπολής τριχοειδικού πλέγματος της περιοχής της ωχράς σε σύγκριση με την ομάδα ελέγχου.
Η ανάγγεια ζώνη της ωχράς παρουσίασε μικρότερη επιφάνεια και περίμετρο, καθώς και χαμηλότερη κυκλικότητα στους ασθενείς με νόσο του Πάρκινσον, σε σύγκριση με την ομάδα ελέγχου.
Όσον αφορά την περιθηλαία περιοχή, οι ασθενείς με νόσο του Πάρκινσον εμφάνισαν σημαντικά μειωμένη πυκνότητα αιμάτωσης και δείκτη ροής στο περιθηλαίο τριχοειδές πλέγμα συγκριτικά με τους υγιείς συμμετέχοντες.
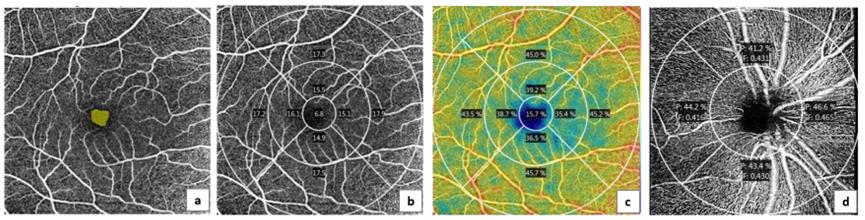
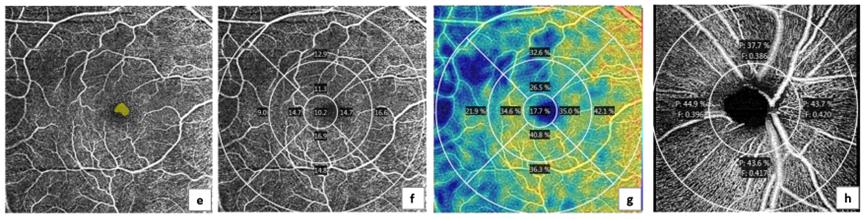
Εικόνα 3. Ενδεικτικές εικόνες της μικροκυκλοφορίας του αμφιβληστροειδούς της περιοχής της ωχράς κηλίδας και του οπτικού νεύρου στο επιφανειακό τριχοειδικό αγγειακό δίκτυο, από άτομο της ομάδας ελέγχου και ασθενή με νόσο του Πάρκινσον. Η OCT-Αγγειογραφία της ωχράς απεικονίζει την ανάγγειο ζώνη (FAZ) και την πυκνότητα (VD) και ροή (FD) στα σημεία της ωχράς, παραωχρικής και περιωχρικής περιοχής, καθώς και την αιμάτωση και ροή του τριχοειδικού αγγειακού δικτύου του οπτικού νεύρου. Ομάδα ελέγχου: a (FAZ), b (VD), c (FD), d (τριχοειδικό δίκτυο οπτικού νεύρου). Ασθενής με PD: e (FAZ), f (VD), g (FD), h (τριχοειδικό δίκτυο οπτικού νεύρου).
Συμπεράσματα
Η παρούσα μελέτη αναδεικνύει μικροαγγειακές αλλοιώσεις του επιπολής τριχοειδικού αγγειακού δικτύου του αμφιβληστροειδούς, τόσο στην ωχρά όσο και στην περιθηλαία περιοχή, σε ασθενείς με πρώιμα στάδια της νόσου του Πάρκινσον. Τα ευρήματά μας υποστηρίζουν ότι η μελέτη των παραμέτρων μικροκυκλοφορίας του αμφιβληστροειδούς με τη χρήση ΟCΤ-Αγγειογραφίας θα μπορούσαν να παρέχουν προγνωστική αξία και να χρησιμοποιηθούν ως βιοδείκτες για τη νόσο του Πάρκινσον, ενισχύοντας τα διαγνωστικά πρωτόκολλα για την πρώιμη ανίχνευση της νόσου, πριν την εμφάνιση εμφανών νευρολογικών συμπτωμάτων.
Acknowledgements: Η παραπάνω μελέτη έχει λάβει το πρώτο βραβείο καλύτερης γραπτής ανακοίνωσης poster στο διεθνές συνέδριο αμφιβληστροειδούς, 12th Floretina ICOOR, Florence, December 2024.
Βιβλιογραφία
- de Lau LM, Breteler MM (2006) Epidemiology of Parkinson’s disease. Lancet Neurol 5(6):525–535
- Chondrogiorgi M, Astrakas LG, Zikou AK, Weis L, Xydis VG, Antonini A, Argyropoulou MI, Konitsiotis S (2019) Multifocal alterations of white matter accompany the transition from normal cognition to dementia in Parkinson’s disease patients. Brain Imaging Behav 13(1):232–240
- Harnois C, Di Paolo T (1990) Decreased dopamine in the retinas of patients with Parkinson’s disease. Invest Ophthalmol Vis Sci 31:2473–2475
- Armstrong RA (2011) Visual symptoms in Parkinson’s disease. Parkinsons Dis 2011:908306
- Maranis S, Tsouli S, Konitsiotis S (2011) Treatment of motor symptoms in advanced Parkinson’s disease: a practical approach. Prog Neuropsychopharmacol Biol Psychiatry 35(8):1795–1807
- Aretouli E, Chondrogiorgi M, Dede O, Koutsonida M, Laf C, Konstantinopoulou E, Kulisevsky J, Kosmidis MH, Konitsiotis S (2021) The Parkinson’s disease-cognitive rating scale: Greek normative data, clinical utility and cultural considerations. J Geriatr Psychiatry Neurol 18:8919887211049110
- Hajee ME, March WF, Lazzaro DR et al (2009) Inner retinal layer thinning in Parkinson disease. Arch Ophthalmol 127(6):737–741
- Guan J, Pavlovic D, Dalkie N et al (2013) Vascular degeneration in Parkinson’s disease. Brain Pathol 23(2):154–164
- Schwartz RS, Halliday GM, Cordato DJ, Kril JJ (2012) Small-vessel disease in patients with Parkinson’s disease: a clinicopathological study. Mov Disord 27(12):1506–1512
- Chalkias IN, Tegos T, Topouzis F, Tsolaki M (2021) Ocular biomarkers and their role in the early diagnosis of neurocognitive disorders. Eur J Ophthalmol 17:11206721211016312
- Wang L, Murphy O, Caldito NG, Calabresi PA, Saidha S (2018) Emerging applications of optical coherence tomography angiography (OCTA) in neurological research. Eye Vis (Lond) 12(5):11
- Asanad S, Mohammed I, Sadun AA, Saeedi OJ (2020) OCTA in neurodegenerative optic neuropathies: emerging biomarkers at the eye-brain interface. Ther Adv Ophthalmol 27(12):2515841420950508