Συντάκτης
Η τοπική κυκλοσπορίνη Α αποτελεί σήμερα τον ακρογωνιαίο λίθο της αντιφλεγμονώδους θεραπείας της οφθαλμικής επιφάνειας, προσφέροντας ασφαλή και αποτελεσματική αντιμετώπιση στο μέτριο-σοβαρό σύνδρομο ξηρού οφθαλμού και άλλες φλεγμονώδεις παθήσεις, με εξαιρετικό προφίλ μακροχρόνιας χρήσης.
Εισαγωγή
Η οφθαλμική επιφάνεια είναι ένα δυναμικό, αλληλεξαρτώμενο σύστημα που περιλαμβάνει τον κερατοειδή, τον επιπεφυκότα, τη δακρυϊκή μεμβράνη, τους μεϊβομιανούς αδένες, τα καλυκοειδή κύτταρα, τα βλέφαρα και το νευρικό πλέγμα του κερατοειδούς. Η σταθερότητα και η υγεία της εξαρτώνται από την ισορροπία μεταξύ παραγωγής, κατανομής και εκροής των δακρύων, καθώς και από την απουσία αυξημένων επιπέδων φλεγμονής. Όταν αυτή η ισορροπία διαταράσσεται, προκύπτουν νοσήματα όπως το σύνδρομο ξηρού οφθαλμού ή Ξηροφθαλμία (Dry Eye Disease – DED) όπως και άλλες φλεγμονώδεις καταστάσεις που επηρεάζουν εκατομμύρια ανθρώπους παγκοσμίως. Πλήττουν από το 5 έως 50% του πληθυσμού ανάλογα με την ηλικία, το φύλο και τη γεωγραφική περιοχή [12], προκαλώντας συμπτώματα, όπως ερεθισμό, καύσο, θολή όραση και πόνο.
Η κυκλοσπορίνη Α (Cyclosporine A – CsA), ένα κυκλικό ενδεκαπεπτίδιο που απομονώθηκε πρώτη φορά το 1971 από τον μύκητα Tolypocladium inflatum, άλλαξε ριζικά την αντιμετώπιση των φλεγμονωδών παθήσεων της οφθαλμικής επιφάνειας. Από ανοσοκατασταλτικό φάρμακο πρώτης γραμμής στις μεταμοσχεύσεις οργάνων, εξελίχθηκε σε τοπικό αντιφλεγμονώδες φάρμακο με έναν ιδιότυπο μηχανισμό δράσης και εξαιρετικό προφίλ ασφάλειας για μακροχρόνια χρήση.[1,2,14]
Παθοφυσιολογία και ο ρόλος της φλεγμονής
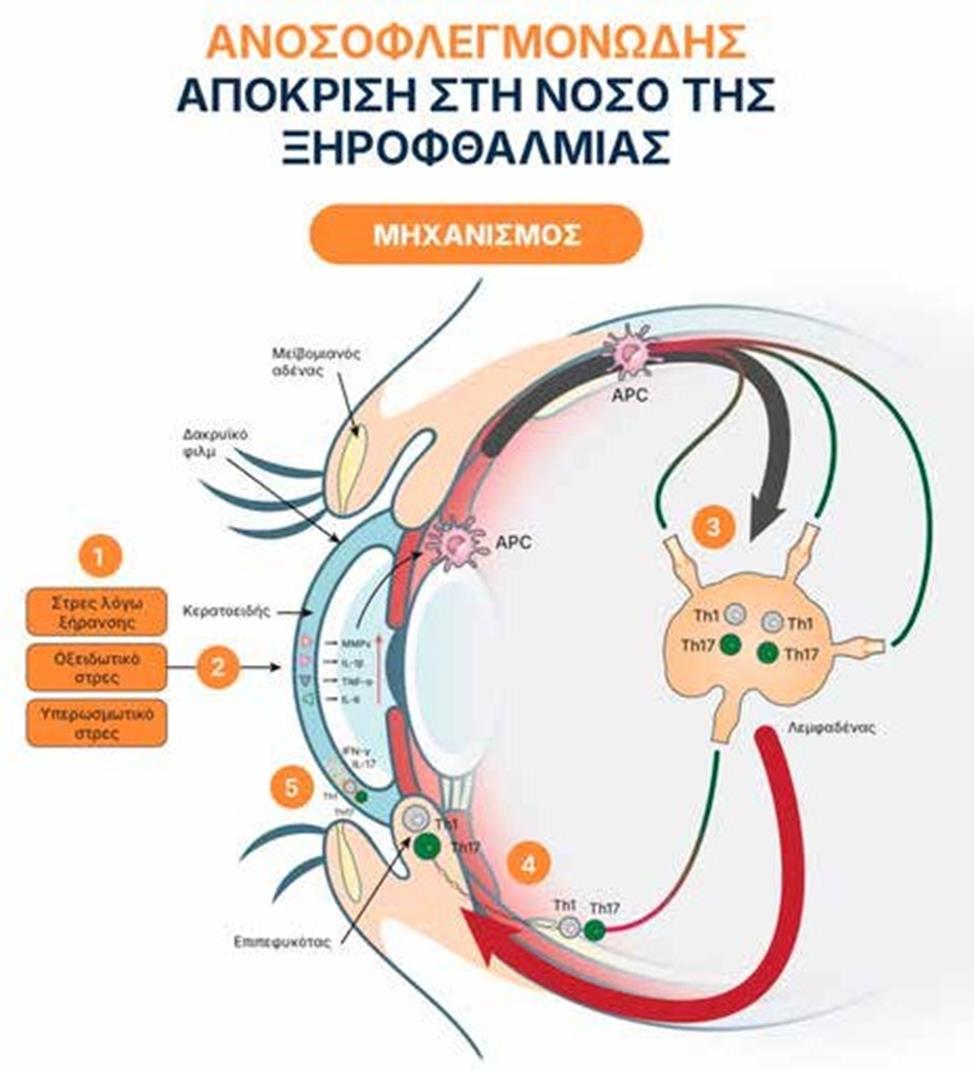
Η σύγχρονη κατανόηση της ξηροφθαλμίας της οφθαλμικής επιφάνειας, όπως περιγράφεται στην TFOS DEWS II (2017), τονίζει ότι η ξηροφθαλμία δεν είναι απλώς μια «έλλειψη δακρύων», αλλά μια φλεγμονώδης νόσος με αυτοενισχυόμενο «φαύλο» κύκλο (Εικόνα 1):
- υπερτονικότητα δακρυϊκής μεμβράνης -> βλάβη επιθηλιακών κυττάρων
- απελευθέρωση προφλεγμονωδών κυτοκινών – ενεργοποίηση δενδριτικών κυττάρων
- ωρίμανση και μετανάστευση Τ-λεμφοκυττάρων στην οφθαλμική επιφάνεια
- περαιτέρω παραγωγή IFN-γ, IL-17, TNF-α -> απόπτωση καλυκοειδών κυττάρων και μεϊβομιανή δυσλειτουργία
- επιδείνωση της αστάθειας της δακρυϊκής μεμβράνης.[1,12]
Η CsA διακόπτει αυτόν τον φαύλο κύκλο στο επίπεδο των Τ-λεμφοκυττάρων.
Μηχανισμός δράσης
Η κυκλοσπορίνη Α (CsA) δρα αναστέλλοντας την ενεργοποίηση των Τ-λεμφοκυττάρων μέσω της δέσμευσης της κυκλοφιλίνης και της επακόλουθης αναστολής της καλσινευρίνης. Αυτό εμποδίζει την παραγωγή προφλεγμονωδών κυτοκινών (κυρίως IL-2, IFN-γ και TNF-α), μειώνοντας τη φλεγμονή στην οφθαλμική επιφάνεια.[1] Στο σύνδρομο ξηρού οφθαλμού, η CsA αυξάνει την πυκνότητα των καλυκοειδών κυττάρων, μειώνει την απόπτωση των επιθηλιακών κυττάρων και βελτιώνει την παραγωγή δακρύων.[1,4] Επιπλέον, επηρεάζει θετικά τη νευρική αναγέννηση του κερατοειδούς και μειώνει τον νευροπαθητικό πόνο.[13] Σε αντίθεση με τα κορτικοστεροειδή, η χρήση της CsA δεν προκαλεί αύξηση της ενδοφθάλμιας πίεσης ή καταρράκτη, καθιστώντας την ιδανική για μακροχρόνια χρήση.[1,12]
Επιγραμματικά η δράση της συνοψίζεται ως εξής:
- Αναστολή καλσινευρίνης: Η CsA δεσμεύεται ενδοκυττάρια από την κυκλοφιλίνη Α, σχηματίζοντας σύμπλοκο που αναστέλλει την φωσφατάση καλσινευρίνη. Αυτό εμποδίζει την αποφωσφορυλίωση και πυρηνική μετατόπιση του παράγοντα μεταγραφής NF-AT, με αποτέλεσμα τη δραστική μείωση της μεταγραφής γονιδίων για τις IL-2, IL-4, IFN-γ και άλλες κυτοκίνες.[1]
- Αποτελέσματα στην οφθαλμική επιφάνεια:
- Αύξηση της πυκνότητας και λειτουργίας καλυκοειδών κυττάρων.
- Μείωση της επιθηλιακής απόπτωσης (μείωση caspase-3, Bax/Bcl-2 ratio).
- Μείωση της έκφρασης HLA-DR και ICAM-1 στα επιφανειακά κύτταρα.
- Μείωση της διήθησης CD3+, CD4+, CD8+ Τ-λεμφοκυττάρων στον επιπεφυκότα.
- Θετική επίδραση στη νευρική αναγέννηση του κερατοειδούς (αύξηση μήκους και πυκνότητας των υποεπιθηλιακών νεύρων σε in vivo confocal microscopy). [4,13]
- Αντιφλεγμονώδης δράση ανεξάρτητη από στεροειδή: Δεν επηρεάζει την παραγωγή προσταγλανδινών, δεν προκαλεί γλαύκωμα ή καταρράκτη, δεν καταστέλλει την επούλωση.[1]
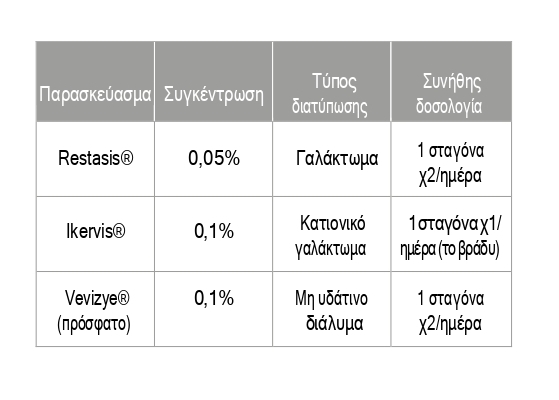
Παρασκευάσματα και Δοσολογία
Σήμερα, διατίθενται πολλαπλά εμπορικά σκευάσματα, όπως το Restasis® (0,05%), το Ikervis® (0,1% κατιονικό γαλάκτωμα) και το πολλά υποσχόμενο Vevizye® (2023) που είναι το πρώτο σκεύασμα με μη υδάτινο διάλυμα σε ημι-υγρό μέσο (perfluorobutylpentane). [3,14,2,7,8,10]
Πρακτικές συμβουλές: ψύξη του φαρμάκου, χρήση τεχνητών δακρύων 10-15 λεπτά πριν την CsA και αφαίρεση φακών επαφής.[2]
Κύριες ενδείξεις και επίπεδα τεκμηρίωσης
Η τοπική CsA είναι εγκεκριμένη και συνιστάται από τις κατευθυντήριες οδηγίες TFOS DEWS II για το μέτριο έως σοβαρό σύνδρομο ξηρού οφθαλμού (επίπεδο 2-3).[12]
- Μέτριο-σοβαρό σύνδρομο ξηρού οφθαλμού (επίπεδο 1A – TFOS DEWS II).[12]
- Ξηροφθαλμία σε σύνδρομο Sjögren (επίπεδο 1B).[11]
- Εαρινή / ατοπική κερατοεπιπεφυκίτιδα (επίπεδο 1B).[5]
- Μετεγχειρητική ξηροφθαλμία (LASIK, καταρράκτης) (επίπεδο 2).[13]
- Νόσος μοσχεύματος έναντι ξενιστή (GVHD) (επίπεδο 2)
- Οφθαλμική ροδόχρους ακμή / δυσλειτουργία μεϊβομιανών αδένων (επίπεδο 2).
- Χρόνια αδενοϊική κερατίτιδα – πρόληψη υποεπιθηλιακών διηθημάτων (επίπεδο 2).
Κλινική αποτελεσματικότητα – πρόσφατα δεδομένα
Δύο βασικές μελέτες φάσης 3 έδειξαν κλινικά σημαντική βελτίωση στο Schirmer Ι και ΙΙ tests, και μείωση της βαφής του επιθηλίου σε σχέση με το placebo.[6] Μακροχρόνια δεδομένα (3 έτη) επιβεβαιώνουν τη διατήρηση της αποτελεσματικότητας της CsA 0,1% και την εξαιρετική ασφάλειά της.[4]
Ειδικά σε ασθενείς με σύνδρομο Sjögren, η CsA 0,1% βελτίωσε σημαντικά τον χρόνο διάσπασης της δακρυϊκής στοιβάδας, το τεστ Schirmer και τον δείκτη ξηρότητας της δακρυϊκης επιφάνειας μετά από 6-12 μήνες.[11]
Πρακτικός οδηγός χορήγησης
- Έναρξη: 1 σταγόνα χ2/ημέρα (Restasis®, Vevizye®) ή χ1 το βράδυ (Ikervis®).
- Διάρκεια: ελάχιστον 6 μήνες για μέγιστο όφελος (καλυκοειδή κύτταρα).
- Συνδυασμοί: Τεχνητά δάκρυα χωρίς συντηρητικά, θερμές κομπρέσες, ω-3, punctal plugs.
- Σε πολύ σοβαρές περιπτώσεις: έναρξη με κορτικοστεροειδείς σταγόνες (loteprednol ή fluorometholone) για 2-4 εβδομάδες + CsA από την πρώτη μέρα -> σταδιακή μείωση των στεροειδών.
- Συμβουλές για μείωση του καύσου κατά την ενστάλαξη: ψύξη φιαλιδίου, τεχνητά δάκρυα 10 λεπτά πριν, «shake & tap» τεχνική.
Παρενέργειες και διαχείριση
Οι συχνότερες ανεπιθύμητες ενέργειες είναι το παροδικό τσούξιμο και καύσος (17-30%), που συνήθως υποχωρούν μετά τις πρώτες εβδομάδες.[3,6] Σπάνια αναφέρονται η επιπεφυκιδική υπεραιμία, θολή όραση ή αίσθημα ξένου σώμα- τος. Δεν έχει παρατηρηθεί αύξηση ενδοφθάλμιας πίεσης ή καταρράκτης ακόμα και μετά από 3-5 έτη χρήσης.[4]
Σύγκριση με εναλλακτικές θεραπείες
Σε σύγκριση με το lifitegrast 5% (Xiidra®), η CsA δείχνει παρόμοια ή καλύτερη αποτελεσματικότητα σε αντικειμενικές παραμέτρους και καλύτερη ανοχή.[9] Σε σχέση με τα κορτικοστεροειδή, η CsA είναι ασφαλέστερη για μακροχρόνια χρήση και μπορεί να χρησιμοποιηθεί ως steroid-sparing παράγοντας.[1,12]
Η CsA παραμένει η μόνη εγκεκριμένη μακροχρόνια αντιφλεγμονώδης θεραπεία με δεδομένα ασφαλείας > 15 ετών. [9,12]
Μελλοντικές κατευθύνσεις (2025-2030)
Νέα παρασκευάσματα χωρίς συντηρητικά, water-free (π.χ. Vevizye®), και συστήματα παρατεταμένης αποδέσμευσης (π.χ. OTX-CSI) βρίσκονται σε προχωρημένο στάδιο κλινικών δοκιμών. Επιπλέον, συνδυασμοί CsA με άλλα μόρια (π.χ. anti-IL-17, JAK inhibitors) ερευνώνται για ανθεκτικές περιπτώσεις.[14]
- Συστήματα παρατεταμένης αποδέσμευσης: OTX-CSI (εμφύτευμα 3-6 μηνών), ENV515 (travoprost + CsA), κλινικές φάσης ΙΙ/ΙΙΙ.
- Συνδυασμοί: CsA + anti-IL-17 ή JAK inhibitors για ανθεκτικές περιπτώσεις.
- Γονιδιακή θεραπεία: φορείς AAV για τοπική έκφραση ανοσοτροποποιητικών πεπτιδίων.
- Εξατομικευμένη ιατρική: βιοδείκτες (MMP-9, HLA-DR, IL-17 στα δάκρυα) για επιλογή ασθενών που θα ωφεληθούν περισσότερο.
Συμπέρασμα
Η τοπική κυκλοσπορίνη Α (CsA) αποτελεί σήμερα την πιο τεκμηριωμένη, ασφαλή και αποτελεσματική αντιφλεγμονώδη θεραπεία για το μέτριο/σοβαρό σύνδρομο ξηρού οφθαλμού και πολλές άλλες φλεγμονώδεις παθήσεις της οφθαλμικής επιφάνειας. Από το 2003 έως το 2025, η εξέλιξη των παρασκευασμάτων βελτίωσε δραστικά τη βιοδιαθεσιμότητα, την ανοχή και την ευκολία χρήσης, ενώ με τη καλύτερη κατανόηση του μηχανισμού δράσης της, η χρήση της επεκτάθηκε και πέρα από την κλασική ανοσοκαταστολή. Στο μέλλον, νέα συστήματα χορήγησης και συνδυαστικές θεραπείες αναμένεται να ενισχύσουν περαιτέρω τη θέση της ως θεραπεία πρώτης γραμμής, βελτιώνοντας σημαντικά την ποιότητα ζωής εκατομμυρίων ασθενών παγκοσμίως.
Η τοπική κυκλοσπορίνη Α (CsA) αποτελεί σήμερα τον ακρογωνιαίο λίθο της αντιφλεγμονώδους θεραπείας της οφθαλμικής επιφάνειας. Με υψηλό προφίλ ασφάλειας και τεκμηριωμένη μακροχρόνια αποτελεσματικότητα, η CsA θα συνεχίσει να κατέχει κεντρική θέση στη θεραπευτική φαρέτρα του οφθαλμιάτρου για τα επόμενα χρόνια.
Βιβλιογραφία
- de Paiva CS, Pflugfelder SC. Immunomodulatory and Anti-Inflammatory Effects of Cyclosporine in Dry Eye Disease. Current Opinion in Ophthalmology 2022;33(6):522-529.
- Baudouin C, Figueiredo FC, Messmer EM, et al. Topical cyclosporine A in ocular surface diseases: A comprehensive review of clinical uses and new formulations. European Journal of Ophthalmology 2023;33(1):8-25.
- Wan KH, Chen LJ, Young AL. Efficacy and safety of different formulations of topical cyclosporine A for dry eye disease: A systematic review and Bayesian network meta-analysis. British Journal of Ophthalmology 2024;108(4):492-501.
- Sheppard JD, Donnenfeld ED, Holland EJ, et al. Long-term topical cyclosporine A 0.05% in severe dry eye disease: 3-year results of a prospective study. The Ocular Surface 2021;22:149-157.
- Leonardi A, Van Dooremaal JC, Labbé A, et al. Once-daily cyclosporine A 0.1% cationic emulsion (Ikervis®) in severe vernal keratoconjunctivitis and atopic keratoconjunctivitis: 12-month results. Acta Ophthalmologica 2022;100(4):e912-e920.
- Sall K, Stevenson OD, Mundorf TK, Reis BL; CsA Phase 3 Study Group. Two multicenter, randomized studies of the efficacy and safety of cyclosporine ophthalmic emulsion in moderate to severe dry eye disease. Ophthalmology 2000;107(4):631-639.
- Tauber J, Schechter BA, Bacharach J, et al. A Phase II/III, randomized, double-masked, vehicle-controlled, dose-ranging study of the efficacy and safety of OTX-101 (0.09% cyclosporine nanomicellar solution) in dry eye disease. Clinical Ophthalmology 2020;14:1437-1448.
- Goldberg DF, Malhotra RP, Simpson RG, et al. Efficacy and safety of cyclosporine A cationic emulsion in the treatment of severe dry eye disease: 12-month results. Journal of Ocular Pharmacology and Therapeutics 2021;37(7):402-410.
- Holland EJ, Luchs J, Karpecki PM, et al. Lifitegrast for the treatment of dry eye disease in adults: Results from five randomized controlled trials. Ophthalmology 2022;129(5):537-549.
- Periman LM, Perez VL, Holden BA, et al. Cyclosporine A 0.09% nanomicellar solution (Cequa®) for dry eye disease: Pooled analysis of two phase 3 studies. Clinical Ophthalmology 2023;17:135-145.
- Labetoulle M, Baudouin C, Calonge M, et al. Role of cyclosporine A 0.1% cat- ionic emulsion in the management of dry eye disease associated with Sjögren’s syndrome: European expert consensus. Journal Français d’Ophtalmologie 2023;46(3):268-279.
- Craig JP, Nichols KK, Akpek EK, et al. TFOS DEWS II Management and Therapy Report. The Ocular Surface 2017;15(3):575-628.
- Kim M, Lee Y, Eom Y, et al. Efficacy of topical 0.05% cyclosporine A in the treatment of post-LASIK dry eye and corneal neuropathy: A prospective study. Cornea 2024;43(2):178-185.
- Gupta PK, Venkateswaran N, O’Neil EC, et al. Emerging therapies in dry eye dis- ease: The role of novel cyclosporine formulations. Current Opinion in Ophthalmology 2025;36(1):45-52.
- Akpek EK, Bunya VY, et al. Vevye (cyclosporine ophthalmic solution 0.1%), water-free: Results of phase 3 clinical trials. American Journal of Ophthalmology 2024;258:112-121.